
소아청소년과 이영목·나지훈 교수
희귀 유전성질환
척수성 근위축증(SMA)
치료제 뉴시너센
소아청소년과 연구팀이 희귀 유전성질환 척수성 근육위축증(SMA) 치료제인 뉴시너센의 효능과 안전성에 대한 임상 결과를 발표했다. 발병 초기에 투여할수록, 치료가 지속될수록 실질적인 운동기능이 개선되는 것으로 나타났다.
글 이영목·나지훈 소아청소년과 교수 / 사진 송인호

척수성 근육위축증(Spinal Muscular Atrophy, SMA)은 상염색체 열성 질환으로, 5q염색체 내 돌연변이가 원인인 신경근육계 희귀질환이다. SMA는 유전적 원인이 규명된 질환으로, 운동신경세포의 생존에 필요한 특수 단백질을 생산하는 유전자의 결손이나 변이에 의해 발생한다. 5q 염색체 내 돌연변이가 발생하면 척수의 전각세포나 뇌간핵의 변성 또는 소실이 발생하면서 진행성 근육 쇠약 및 근육 소모가 일어난다.
SMA는 발생 시기와 운동 발달 상태에 따라 분류하며, 이는 예후와 연관이 있다. SMA Type Ⅰ은 생후 6개월 미만에서 증상이 발생하며, 독립적으로 앉지 못하며 기대여명은 2세 미만으로 알려져 있다. SMA Type Ⅱ는 생후 6~18개월에서 증상이 발생하며 독립적으로 앉을 수는 있지만, 서지는 못하고 기대여명은 10~40세 정도로 알려져 있다. SMA Type Ⅲ은 생후 18개월 초과에서 증상이 발생하며 독립적으로 서 있을 수는 있지만, 걷지는 못하며 기대여명은 일반적인 정상 성인과 거의 같다고 알려져 있다.
시기에 따른 적절한 치료 필요
SMA는 진행성 질환이므로 시기에 따라 적절한 치료가 필요하다. 조기에 치료할수록 더 좋은 예후를 기대할 수 있기 때문에 집중치료 프로그램 등 적극적인 치료적 중재가 필요하다. 유전자 기반 치료제인 뉴시너센(Nusinersen)은 2016년 10월에 미국 FDA 승인을 받았고, 2017년 12월에는 한국 식품의약품안전처 승인을 받았다. 2019년 4월부터 보험급여가 적용돼, 현재 사용 중이다. 뉴시너센은 Anti-Sense Oligonucleotide(ASO) 제제로, SMN1 gene의 back-up 유전자인 SMN2 gene의 pre-mRNA에 결합해 splicing을 억제하는 인자를 대체하고 Exon 7의 손실 없이 온전한 단백질을 만들어낼 수 있게 돕는 역할을 한다.
강남세브란스병원 SMA 연구팀은 2019년 3월부터 2022년 4월까지, 약 3년간 강남세브란스병원에서 진단받고 뉴시너센 치료를 진행한 SMA type Ⅰ, Ⅱ 환자 30명의 임상적 특징 및 치료 경과를 보고했다. 그 결과, 환자들에게 증상이 발병한 나이는 평균 1.2세, 90%가 SMA type Ⅱ였으며, 87%에 대하여 CT 중재를 통한 약물 주입 치료를 진행했다.
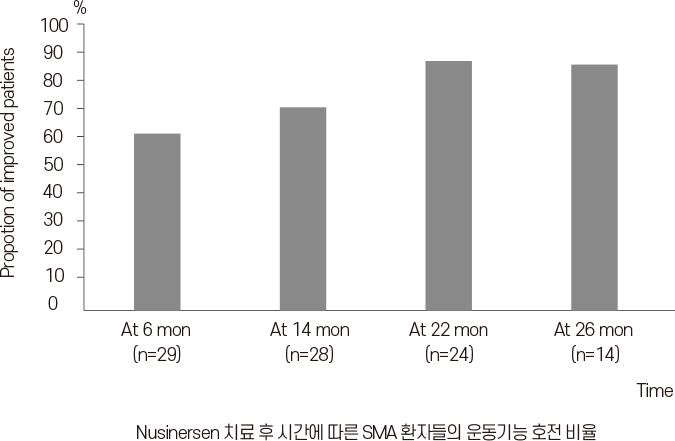
치료를 받고 6개월, 14개월, 22개월, 26개월 경과된 시점에서 운동기능이 향상된 환자는 각각 72%, 71%, 88%, 86%였다. SMA 환자들의 운동기능을 측정하는 HFMSE(Hammersmith Functional Motor Scale-Expanded) score는 치료 기간이 길수록 높아졌다(6개월-평균 2.1점 증가, 14개월-2.88점, 22개월-4.21점, 26개월-5.29점).
즉, 강남세브란스병원에서 뉴시너센 치료를 진행한 SMA 환자 30명(고위험군 포함)은 유의미한 운동기능 향상을 보였다. 치료 과정에서 1~2일 정도 가벼운 부작용은 있었지만, 심각한 부작용은 관찰되지 않아 치료가 안전하게 진행됨을 보고했다.
유전자 기반 치료제 안정성과
효용성 입증
해외 연구에서 SMA 환자들에게 여러 치료 방법에 따른 효능 및 안정성은 이미 발표된 바 있다. 그러나 국내 소아청소년이 포함된 환자 데이터는 현재까지 보고된 것이 없고, 단일 기관 연구는 제한적이며, 척추측만증 수술 과거력이 있거나 호흡 보조가 필요한 중증 SMA 환자들까지 포함된 연구는 극히 드문 것이 현실이다.
따라서 희귀질환인 SMA 치료 경험을 정리해 SMA 환자들의 치료 방법에 따른 효능 및 안정성에 대한 연구 결과를 보고하는 것은 SMA를 연구 및 치료하는 전 세계 학자들에게 좋은 참고문헌을 제공할 수 있다. 이번 연구는 SMA 환자에게 뉴시너센 치료는 안전하고 효과적이라는 것을 증명했으며, 이들에게 뉴시너센과 같은 유전자 기반 치료제의 도입이 더욱 적극적으로 이루어져야 한다는 것을 시사한다. 또 뉴시너센의 치료 결과를 평가할 운동기능을 좀 더 민감하게 측정할 수 있는 진단 프로토콜의 필요성 또한 역설하고 있다.

유전자 기반 치료제 개발과
관련 연구에 기대
뉴시너센을 비롯한 유전자 기반 치료제들이 더욱 발전되어 개발되고 있다. 졸겐스마(성분명: Onasemnogene abeparvovec)는 바이러스벡터를 활용하여 SMN1 gene을 활성화한다. 이 외에도 유전자 편집 기술을 활용한 유전자 기반 치료제들이 앞으로 기대되고 있다. 수많은 유전자 관련 질환의 치료에 뉴시너센과 같은 유전자 기반 치료제들을 적용하면 앞으로 수많은 환자의 치료에 크게 기여할 것이며, 유전자 이상으로 인한 수많은 질환의 치료 표준이 될 것으로 전망된다.
또 HFMSE 점수가 모든 SMA 환자의 운동기능을 정확하게 측정할 수는 없어서 더욱 정확한 운동기능 평가방법이 필요하다. HFMSE를 통해서 뉴시너센을 투여한 모든 SMA 환자의 운동기능 호전 상태를 측정할 수 없어서 뉴시너센 재투여 자격조건에 해당되지 못하는 경우가 많았기 때문이다.
앞으로의 연구에서는 뉴시너센 이후 새로 개발된 졸겐스마나 경구투여제인 리스디플람(Risdiplam)을 투여했을 때 환자의 운동기능이 개선되는 효과를 다루어야 할 것이다. 그리고 운동기능 외에도 신경근육계가 관여되어 있는 호흡 기능이나 소화 기능, 영양 상태 등의 호전을 확인하는 연구도 필요하기 때문에 이와 관련된 향후 연구가 주목되고 기대된다.






